Lùi thời hạn cấp phép lưu hành vaccine Pfizer trên trẻ em dưới 5 tuổi thêm 2 tháng
Cơ quan quản lý dược phẩm và thực phẩm Mỹ (FDA) cần có thêm các dữ liệu để đánh giá tác động cũng như hiệu quả của vaccine ngừa COVID-19 của hãng dược Pfizer/BioNTech để sử dụng trên đối tượng là các trẻ em dưới 5 tuổi trong 2 tháng tới.
- Bộ Y tế tổ chức thí điểm tiêm vaccine cho trẻ em trước khi triển khai diện rộng
- Cập nhật tình hình dịch COVID-19: WHO hy vọng sẽ có 230 triệu liều vaccine cho châu Phi
- Sự khác nhau giữa vaccine cho người lớn và trẻ em
Theo quyết định mới nhất của Mỹ thì việc cấp phép sử dụng vaccine ngừa COVID-19 của Pfizer/BioNTech cho trẻ nhỏ dưới 4 tuổi sẽ phải trì hoãn ít nhất 2 tháng sau khi FDA tuyên bố cần thêm các dữ liệu thử nghiệm để đưa ra khuyến nghị chính thức.
Trong tuyên bố ngày 11/2, FDA cho biết cơ quan này đã đánh giá các thông tin mới từ cuộc thử nghiệm mà Pfizer/BioNTech đã gửi kèm cùng với đơn xin cấp phép, tuy nhiên cơ quan này khẳng định cần thêm nhiều dữ liệu đánh giá hơn trước khi có quyết định.
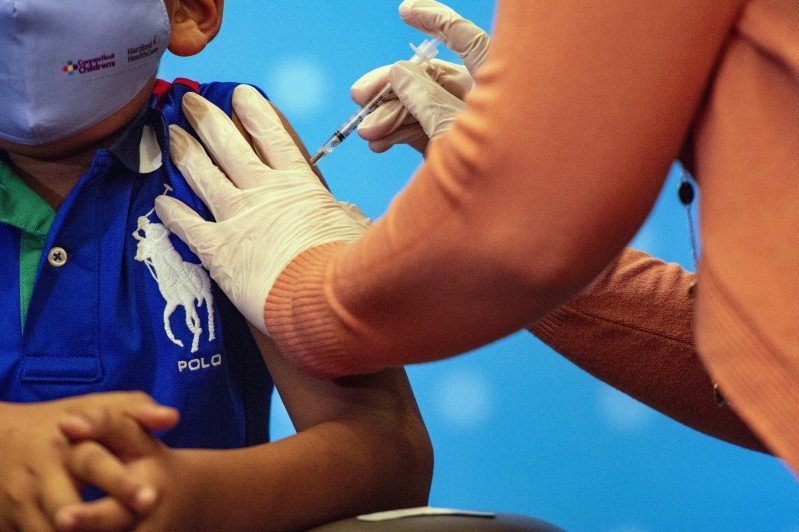
Trẻ em dưới 5 tuổi là đối tượng nhạy cảm với các thay đổi nên việc cấp phép lưu hành vaccine ngừa COVID-19 sẽ cần phải có thêm dữ liệu để đánh giá.
Theo kế hoạch trước đó, FDA dự định trong tuần tới sẽ đưa ra ra khuyến nghị sử dụng loại vaccine trên cho trẻ sơ sinh và trẻ từ 6 tháng tuổi đến 4 tuổi và Chính phủ Mỹ sẽ triển khai chương trình tiêm chủng dành cho trẻ nhỏ từ ngày 21/2.
FDA trước đó đã yêu cầu Pfizer đẩy nhanh quá trình xin cấp phép sử dụng vaccine ngừa COVID-19 cho nhóm trẻ nhỏ này do biến thể Omicron đang làm gia tăng số ca nhiễm mới, đặc biệt ở trẻ em.
Đầu tháng 2, Pfizer/BioNTech đã xúc tiến quy trình cấp phép sử dụng vaccine ngừa COVID-19 của hãng cho nhóm đối tượng trẻ nhỏ theo yêu cầu của FDA. Tuy nhiên, hãng dược phẩm này không công khai dữ liệu đánh giá về hiệu quả của vaccine họ đối với nhóm đối tượng này.
Việc Pfizer/BioNTech đẩy nhanh việc xin cấp phép là khá bất ngờ bởi hồi tháng 12/2021, hai công ty dược phẩm này ra thông báo cho biết hiệu quả thử nghiệm không được như mong muốn và hãng sẽ điều chỉnh các cuộc thử nghiệm với mũi 3. Trong tuyên bố ngày 11/2, Pfizer/BioNTech cho biết đến đầu tháng 4, hãng mới có được dữ liệu đánh giá từ thử nghiệm mũi 3 này.
Tiến sĩ Peter Marks, Giám đốc Trung tâm đánh giá và nghiên cứu sinh học của FDA trấn an các bậc phụ huynh về sự chậm trễ này, nhấn mạnh cơ quan này cần thêm thời gian để đưa ra quyết định vì muốn đảm bảo vaccine phải đạt mọi tiêu chuẩn về an toàn và hiệu quả khi được cấp phép sử dụng.
Theo Tạp chí Điện tử























Tối thiểu 10 chữ Tiếng việt có dấu Không chứa liên kết
Gửi bình luận